東レ・メディカルは6日、新たな多用途透析装置「個人用透析装置TR‐20EX」を静岡工場(静岡県沼津市)で開発し、厚生労働省の製造販売承認を取得して今月から販売を開始したと発表した。
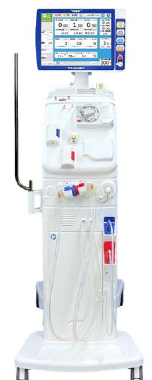
同装置は、現在国内医療機関で使用されている「TR‐3300S」の後継機種で、「透析用監視装置TR‐10EX」の個人用タイプ。現在、同社が掲げる「EXソリューション」(診療支援、業務支援、経済性)において、「診療支援」「業務支援」に寄与する新たなEXシリーズとなる。
液晶ディスプレイの
2024年6月7日
2024年4月12日
2024年4月8日
2024年3月26日
2024年2月28日
2023年12月19日
2023年10月24日
2023年9月27日
2023年6月27日
2023年6月14日